第2节 氧化与燃烧 学案(含答案)
图片预览



文档简介
1113790011188700第2节 氧化与燃烧
一、氧化反应
1.定义:物质跟氧反应叫做氧化反应。
2.类型:A、缓慢氧化:氧化过程中进行得非常缓慢,甚至在短期内不易察觉,如钢铁生锈,生物呼吸作用等。
B、剧烈氧化:氧化过程进行得很剧烈,如硫、铁磷等物质的燃烧。
注:(1)物质跟氧发生的反应,叫做氧化反应,不能将氧改为氧气,否则会将氧化反应的范围缩小。
(2)物质跟氧气发生的化学反应一定是氧化反应。
例1、下列变化中属于缓慢氧化的是 ( )
A.木炭燃烧 B.食物腐败 C.蜡烛燃烧 D.汽油燃烧
例2、下列变化不属于氧化反应的是 ( )
A.铁生锈 B.镁条燃烧
C.高锰酸钾制氧气 D.食物腐烂
例3、物质在空气中燃烧或缓慢氧化,其共同点是 ( )
①都产生热量 ②都发光 ③都是氧化反应 ④都需要点燃
A.①② B.①③ C.③④ D.①②③④
例4、下列反应中属于氧化反应的是 (填字母,下同),属于化合反应的是 。?
A.铜+氧气氧化铜
B.氨气+氧气一氧化氮+水
C.氢气+氧气水
D.甲烷+氧气水+二氧化碳
E.氢气+氯气氯化氢
F.一氧化碳+氧气二氧化碳
二、燃烧的条件
1.燃烧:可燃物与空气中的氧气发生的一种发光、发热、剧烈的氧化反应。
A、条件:a有可燃物;b要有助燃剂,常用助燃剂为氧气;c温度达到该可燃物的着火点。
2.爆炸:如果燃烧以极快的速度在有限的空间里发生,瞬间积累大量的热,使气体体积急剧的膨胀,就会引起爆炸。
A、分类:a、燃烧引起的爆炸,实质是可燃物与氧气发生氧化反应生成的气体在有限空间内急剧膨胀,引起爆炸,是化学反应。
b、在有限空间内气体受热膨胀引起爆炸,没有新物质生成,是物理变化,如车胎爆炸。
3.自燃:物质在缓慢氧化过程中产生的热量不能及时散热,就会越积越多,使温度逐渐升高,当温度升高到可燃物的着火点时,如果再遇上充足的氧气,物质会自发的燃烧起来。这种由缓慢引起的自发燃烧叫自燃。
4.常见的自燃:一些着火点较低的可燃物,如粮食、麦秆、煤炭和棉纱等,如果堆放不合理,空气不流通,时间久了极易自燃,引发火灾。
5. 燃烧、爆炸、缓慢氧化和自燃的关系
例1、如图所示的实验可用于探究燃烧的条件,下列说法正确的是( )
A.对比②③,可以得出白磷、红磷的着火点不同
B.对比①③,可以得出燃烧需要可燃物
C.对比①②,可以得出燃烧需要氧气
D.即使给②中的白磷通入氧气,燃烧也一定不能发生
例2、小金对物质燃烧知识进行了整理并探究。
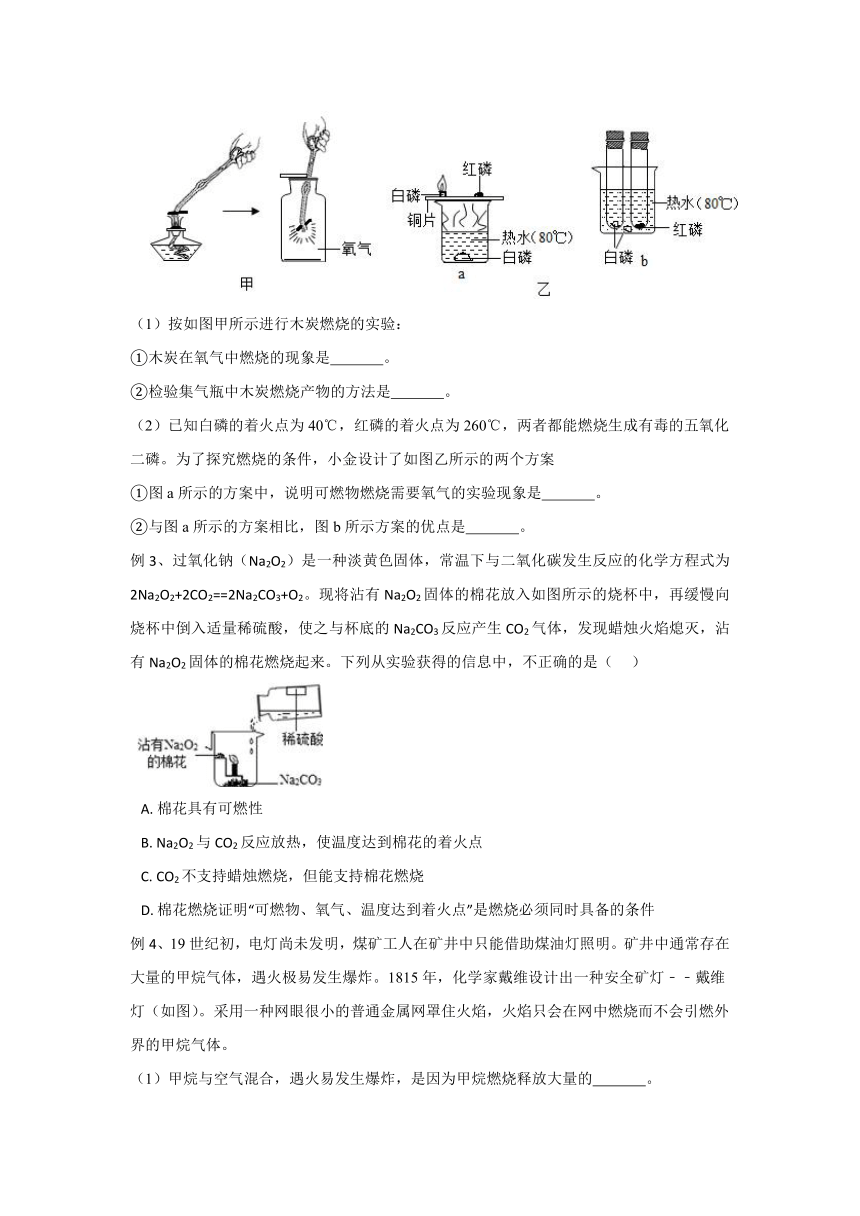
(1)按如图甲所示进行木炭燃烧的实验:
①木炭在氧气中燃烧的现象是 。
②检验集气瓶中木炭燃烧产物的方法是 。
(2)已知白磷的着火点为40℃,红磷的着火点为260℃,两者都能燃烧生成有毒的五氧化二磷。为了探究燃烧的条件,小金设计了如图乙所示的两个方案
①图a所示的方案中,说明可燃物燃烧需要氧气的实验现象是 。
②与图a所示的方案相比,图b所示方案的优点是 。
例3、过氧化钠(Na2O2)是一种淡黄色固体,常温下与二氧化碳发生反应的化学方程式为2Na2O2+2CO2==2Na2CO3+O2。现将沾有Na2O2固体的棉花放入如图所示的烧杯中,再缓慢向烧杯中倒入适量稀硫酸,使之与杯底的Na2CO3反应产生CO2气体,发现蜡烛火焰熄灭,沾有Na2O2固体的棉花燃烧起来。下列从实验获得的信息中,不正确的是(??? )
A.?棉花具有可燃性
B.?Na2O2与CO2反应放热,使温度达到棉花的着火点
C.?CO2不支持蜡烛燃烧,但能支持棉花燃烧
D.?棉花燃烧证明“可燃物、氧气、温度达到着火点”是燃烧必须同时具备的条件
例4、19世纪初,电灯尚未发明,煤矿工人在矿井中只能借助煤油灯照明。矿井中通常存在大量的甲烷气体,遇火极易发生爆炸。1815年,化学家戴维设计出一种安全矿灯﹣﹣戴维灯(如图)。采用一种网眼很小的普通金属网罩住火焰,火焰只会在网中燃烧而不会引燃外界的甲烷气体。
(1)甲烷与空气混合,遇火易发生爆炸,是因为甲烷燃烧释放大量的 。
(2)用戴维灯照明,不会引燃矿井中的甲烷,原因是 。
例5、如图是为探究物质燃烧条件而设计的实验。甲中的白磷未燃烧,而乙中的白磷燃烧。
(1)该实验主要探究的燃烧条件是 。?
(2)白磷燃烧的产物与红磷相同,为什么不用红磷去替代白磷?请说明理由:?
。?
(3)如仅用该装置进行实验,验证空气中氧气的体积分数约为20%,应做到:①白磷 ;
②将锥形瓶 。?
三、灭火与火灾自救
1.灭火原理:A清除可燃物或使可燃物与其他可燃物隔离;
B使可燃物与空气(氧气)隔离;
C降低可燃物的温度到着火点以下。
注:灭火时降低的是可燃物的温度而不是可燃物的着火点。
只要破坏燃烧的三个条件中的任意一个,即可达到灭火目的。
2. 几种常用灭火器的适用范围
(1)泡沫灭火器:用来扑灭木材、棉布等燃烧而引起的失火。
(2)干粉灭火器:除用来扑灭一般失火外,还可用来扑灭油、气等燃烧引起的失火。
(3)液态二氧化碳灭火器:用来扑灭图书档案、贵重设备、精密仪器等的失火。使用时一定要先将手握在钢瓶的木柄上,否则会把手冻伤。
3. 几种常见的灭火方法
灭火的方法
目的
①用水灭火;②吹灭蜡烛;③油锅失火倒入要炒的菜
降低温度
①用灯帽盖灭酒精灯;②油锅失火用锅盖盖灭;③实验台上酒精着火用湿抹布盖灭
隔绝氧气
①森林灭火,开辟隔离带;②关闭煤气灶阀门
移走可燃物
例1、2018年11月8日,美国加州发生特大型火灾,历时半月才将其基本扑灭。下列关于森林火灾应急措施或原因不合理的是( )
A.砍掉或清理大火前面的干枯树枝、树叶等可燃物,达到隔离可燃物的目的
B.森林中随意遗弃矿泉水瓶可能会引发火灾
C.紧急疏散火灾周围地区的人群及贵重物品,达到减少损失的目的
D.飞机播撒干冰,达到降低可燃物着火点的目的
例2、2015年5月30日,玉林市消防战士杨科璋为了抢救人民群众的生命财产,献出了年轻的生命.在向英雄致敬的同时,我们必须掌握一些消防安全知识.
(1)如图是探究燃烧条件的部分图示.实验一是探究燃烧需要 ;实验二中原来在热水里不燃烧的白磷,在通入氧气后燃烧了,说明燃烧还需要 .
(2)高楼起火时,消防队员常用高压水枪灭火,此措施依据的灭火原理是 .
例3、如图实验显示了灭火器的原理,下列说法错误的是( )
A.浓盐酸和碳酸钠溶液都是无色液体
B.由实验Ⅰ到实验Ⅱ使锥形瓶倒立的直接目的是让两种液体混合
C.利用实验Ⅱ喷出的大量液体降低可燃物的着火点来灭火
D.主要是利用反应产生的二氧化碳来灭火
例4、面粉是常见的食物,但是大量的面粉浮在空气中也会爆炸,产生危险。如图:拿一个在靠近底部打了一个小孔的八宝粥的空罐子,里面固定并点燃一枝生日蜡烛;另外在一个小塑料盒子里装人面粉;用一用呀管从外而涌人而粉中,盖好盖子,迅速鼓人大量空气。
(1)会发生的实验现象是:
(2)鼓人大量空气的作用是:
(3)爆炸的条件是:
(4)如果你是面粉厂厂长,你如何避免爆炸事故的发生?
请给出可行建议(两条即可): 、
四、放热反应与吸热反应
1、化学反应在生成新物质的同时,还伴随着 的变化,通常表现为热量的变化,即有放热现象或吸热现象。
①放出热量的反应:燃料的燃烧,生石灰与水结合成氢氧化钙,镁与盐酸反应。
②有些化学反应 热量,如碳与二氧化碳在高温条件下生成CO,Ba(OH)2与NH4Cl反应。
2、能量的转化:化学能与热能之间相互转化,与其他形式的能也能相互转化,如电池充电是电能转化为化学能;使用电池是化学能转化成电能。
3、化学反应能量变化大小不同,有些非常细微,只有灵敏的仪器才能检测到,化学反应中能量常表现为热、光、电等。
例1、下列关于化学反应与能量变化的叙述中,正确的是( )
A.人类利用的能量都是通过化学反应获得的
B.在化学反应中只有燃烧反应才能放出热量
C.化学反应过程中都会发生放热现象
D.化学反应伴随有能量变化
例2、如图是关于氧气化学性质的部分知识网络,关于该图的说法正确的是( )
A.S、P在氧气中燃烧均会产生大量白烟 B.Fe在(Ⅰ)(Ⅱ)两类反应中的产物相同
C.(Ⅰ)类反应放出热量,(Ⅱ)类反应吸收热量 D.(Ⅰ)(Ⅱ)两类反应均体现了氧气的氧化性
例3、如图是同学们探究物质燃烧条件的部分装置图。向烧杯中加入适量水,一段时间后,试管中的白磷被引燃。
(1)上述实验现象说明了生石灰和水反应是 (填“放热”或“吸热”)反应。?
(2)实验中涉及的两个化学反应都属于基本反应类型中的 反应。?
参考答案:
1、例1、B例2、C例3、B
例4、ABCDF ACEF
2、例1、C
例2、发出白光,放出热量;反应结束后,向瓶中加入澄清石灰水,石灰水变浑浊,说明是二氧化碳;铜片上的白磷燃烧,热水中的白磷不能燃烧;无污染;
例3、C
例4、热量;戴维灯采用一种网眼很小的普通金属网罩住火焰,由于金属能够吸收热量并散放到空气中,使金属周围的温度降低,甲烷的温度达不到着火点,所以不会引燃外界的甲烷气体
例5、(1)燃烧需要氧气 (2)红磷的着火点比白磷高,热水的温度达不到红磷的着火点
(3)①必须足量 ②密封好,多次倒置(合理即可)
3、例1、D
例2、可燃物;氧气;降低温度到可燃物的着火点以下,隔绝空气;
例3、C
例4、(1)爆炸
(2)吹散面粉,使面粉充满罐子
(3)在密闭的空间内剧烈燃烧
(4)严禁烟火;开窗通风
4、例1、D
例2、D
例3、(1)放热 (2)化合
一、氧化反应
1.定义:物质跟氧反应叫做氧化反应。
2.类型:A、缓慢氧化:氧化过程中进行得非常缓慢,甚至在短期内不易察觉,如钢铁生锈,生物呼吸作用等。
B、剧烈氧化:氧化过程进行得很剧烈,如硫、铁磷等物质的燃烧。
注:(1)物质跟氧发生的反应,叫做氧化反应,不能将氧改为氧气,否则会将氧化反应的范围缩小。
(2)物质跟氧气发生的化学反应一定是氧化反应。
例1、下列变化中属于缓慢氧化的是 ( )
A.木炭燃烧 B.食物腐败 C.蜡烛燃烧 D.汽油燃烧
例2、下列变化不属于氧化反应的是 ( )
A.铁生锈 B.镁条燃烧
C.高锰酸钾制氧气 D.食物腐烂
例3、物质在空气中燃烧或缓慢氧化,其共同点是 ( )
①都产生热量 ②都发光 ③都是氧化反应 ④都需要点燃
A.①② B.①③ C.③④ D.①②③④
例4、下列反应中属于氧化反应的是 (填字母,下同),属于化合反应的是 。?
A.铜+氧气氧化铜
B.氨气+氧气一氧化氮+水
C.氢气+氧气水
D.甲烷+氧气水+二氧化碳
E.氢气+氯气氯化氢
F.一氧化碳+氧气二氧化碳
二、燃烧的条件
1.燃烧:可燃物与空气中的氧气发生的一种发光、发热、剧烈的氧化反应。
A、条件:a有可燃物;b要有助燃剂,常用助燃剂为氧气;c温度达到该可燃物的着火点。
2.爆炸:如果燃烧以极快的速度在有限的空间里发生,瞬间积累大量的热,使气体体积急剧的膨胀,就会引起爆炸。
A、分类:a、燃烧引起的爆炸,实质是可燃物与氧气发生氧化反应生成的气体在有限空间内急剧膨胀,引起爆炸,是化学反应。
b、在有限空间内气体受热膨胀引起爆炸,没有新物质生成,是物理变化,如车胎爆炸。
3.自燃:物质在缓慢氧化过程中产生的热量不能及时散热,就会越积越多,使温度逐渐升高,当温度升高到可燃物的着火点时,如果再遇上充足的氧气,物质会自发的燃烧起来。这种由缓慢引起的自发燃烧叫自燃。
4.常见的自燃:一些着火点较低的可燃物,如粮食、麦秆、煤炭和棉纱等,如果堆放不合理,空气不流通,时间久了极易自燃,引发火灾。
5. 燃烧、爆炸、缓慢氧化和自燃的关系
例1、如图所示的实验可用于探究燃烧的条件,下列说法正确的是( )
A.对比②③,可以得出白磷、红磷的着火点不同
B.对比①③,可以得出燃烧需要可燃物
C.对比①②,可以得出燃烧需要氧气
D.即使给②中的白磷通入氧气,燃烧也一定不能发生
例2、小金对物质燃烧知识进行了整理并探究。
(1)按如图甲所示进行木炭燃烧的实验:
①木炭在氧气中燃烧的现象是 。
②检验集气瓶中木炭燃烧产物的方法是 。
(2)已知白磷的着火点为40℃,红磷的着火点为260℃,两者都能燃烧生成有毒的五氧化二磷。为了探究燃烧的条件,小金设计了如图乙所示的两个方案
①图a所示的方案中,说明可燃物燃烧需要氧气的实验现象是 。
②与图a所示的方案相比,图b所示方案的优点是 。
例3、过氧化钠(Na2O2)是一种淡黄色固体,常温下与二氧化碳发生反应的化学方程式为2Na2O2+2CO2==2Na2CO3+O2。现将沾有Na2O2固体的棉花放入如图所示的烧杯中,再缓慢向烧杯中倒入适量稀硫酸,使之与杯底的Na2CO3反应产生CO2气体,发现蜡烛火焰熄灭,沾有Na2O2固体的棉花燃烧起来。下列从实验获得的信息中,不正确的是(??? )
A.?棉花具有可燃性
B.?Na2O2与CO2反应放热,使温度达到棉花的着火点
C.?CO2不支持蜡烛燃烧,但能支持棉花燃烧
D.?棉花燃烧证明“可燃物、氧气、温度达到着火点”是燃烧必须同时具备的条件
例4、19世纪初,电灯尚未发明,煤矿工人在矿井中只能借助煤油灯照明。矿井中通常存在大量的甲烷气体,遇火极易发生爆炸。1815年,化学家戴维设计出一种安全矿灯﹣﹣戴维灯(如图)。采用一种网眼很小的普通金属网罩住火焰,火焰只会在网中燃烧而不会引燃外界的甲烷气体。
(1)甲烷与空气混合,遇火易发生爆炸,是因为甲烷燃烧释放大量的 。
(2)用戴维灯照明,不会引燃矿井中的甲烷,原因是 。
例5、如图是为探究物质燃烧条件而设计的实验。甲中的白磷未燃烧,而乙中的白磷燃烧。
(1)该实验主要探究的燃烧条件是 。?
(2)白磷燃烧的产物与红磷相同,为什么不用红磷去替代白磷?请说明理由:?
。?
(3)如仅用该装置进行实验,验证空气中氧气的体积分数约为20%,应做到:①白磷 ;
②将锥形瓶 。?
三、灭火与火灾自救
1.灭火原理:A清除可燃物或使可燃物与其他可燃物隔离;
B使可燃物与空气(氧气)隔离;
C降低可燃物的温度到着火点以下。
注:灭火时降低的是可燃物的温度而不是可燃物的着火点。
只要破坏燃烧的三个条件中的任意一个,即可达到灭火目的。
2. 几种常用灭火器的适用范围
(1)泡沫灭火器:用来扑灭木材、棉布等燃烧而引起的失火。
(2)干粉灭火器:除用来扑灭一般失火外,还可用来扑灭油、气等燃烧引起的失火。
(3)液态二氧化碳灭火器:用来扑灭图书档案、贵重设备、精密仪器等的失火。使用时一定要先将手握在钢瓶的木柄上,否则会把手冻伤。
3. 几种常见的灭火方法
灭火的方法
目的
①用水灭火;②吹灭蜡烛;③油锅失火倒入要炒的菜
降低温度
①用灯帽盖灭酒精灯;②油锅失火用锅盖盖灭;③实验台上酒精着火用湿抹布盖灭
隔绝氧气
①森林灭火,开辟隔离带;②关闭煤气灶阀门
移走可燃物
例1、2018年11月8日,美国加州发生特大型火灾,历时半月才将其基本扑灭。下列关于森林火灾应急措施或原因不合理的是( )
A.砍掉或清理大火前面的干枯树枝、树叶等可燃物,达到隔离可燃物的目的
B.森林中随意遗弃矿泉水瓶可能会引发火灾
C.紧急疏散火灾周围地区的人群及贵重物品,达到减少损失的目的
D.飞机播撒干冰,达到降低可燃物着火点的目的
例2、2015年5月30日,玉林市消防战士杨科璋为了抢救人民群众的生命财产,献出了年轻的生命.在向英雄致敬的同时,我们必须掌握一些消防安全知识.
(1)如图是探究燃烧条件的部分图示.实验一是探究燃烧需要 ;实验二中原来在热水里不燃烧的白磷,在通入氧气后燃烧了,说明燃烧还需要 .
(2)高楼起火时,消防队员常用高压水枪灭火,此措施依据的灭火原理是 .
例3、如图实验显示了灭火器的原理,下列说法错误的是( )
A.浓盐酸和碳酸钠溶液都是无色液体
B.由实验Ⅰ到实验Ⅱ使锥形瓶倒立的直接目的是让两种液体混合
C.利用实验Ⅱ喷出的大量液体降低可燃物的着火点来灭火
D.主要是利用反应产生的二氧化碳来灭火
例4、面粉是常见的食物,但是大量的面粉浮在空气中也会爆炸,产生危险。如图:拿一个在靠近底部打了一个小孔的八宝粥的空罐子,里面固定并点燃一枝生日蜡烛;另外在一个小塑料盒子里装人面粉;用一用呀管从外而涌人而粉中,盖好盖子,迅速鼓人大量空气。
(1)会发生的实验现象是:
(2)鼓人大量空气的作用是:
(3)爆炸的条件是:
(4)如果你是面粉厂厂长,你如何避免爆炸事故的发生?
请给出可行建议(两条即可): 、
四、放热反应与吸热反应
1、化学反应在生成新物质的同时,还伴随着 的变化,通常表现为热量的变化,即有放热现象或吸热现象。
①放出热量的反应:燃料的燃烧,生石灰与水结合成氢氧化钙,镁与盐酸反应。
②有些化学反应 热量,如碳与二氧化碳在高温条件下生成CO,Ba(OH)2与NH4Cl反应。
2、能量的转化:化学能与热能之间相互转化,与其他形式的能也能相互转化,如电池充电是电能转化为化学能;使用电池是化学能转化成电能。
3、化学反应能量变化大小不同,有些非常细微,只有灵敏的仪器才能检测到,化学反应中能量常表现为热、光、电等。
例1、下列关于化学反应与能量变化的叙述中,正确的是( )
A.人类利用的能量都是通过化学反应获得的
B.在化学反应中只有燃烧反应才能放出热量
C.化学反应过程中都会发生放热现象
D.化学反应伴随有能量变化
例2、如图是关于氧气化学性质的部分知识网络,关于该图的说法正确的是( )
A.S、P在氧气中燃烧均会产生大量白烟 B.Fe在(Ⅰ)(Ⅱ)两类反应中的产物相同
C.(Ⅰ)类反应放出热量,(Ⅱ)类反应吸收热量 D.(Ⅰ)(Ⅱ)两类反应均体现了氧气的氧化性
例3、如图是同学们探究物质燃烧条件的部分装置图。向烧杯中加入适量水,一段时间后,试管中的白磷被引燃。
(1)上述实验现象说明了生石灰和水反应是 (填“放热”或“吸热”)反应。?
(2)实验中涉及的两个化学反应都属于基本反应类型中的 反应。?
参考答案:
1、例1、B例2、C例3、B
例4、ABCDF ACEF
2、例1、C
例2、发出白光,放出热量;反应结束后,向瓶中加入澄清石灰水,石灰水变浑浊,说明是二氧化碳;铜片上的白磷燃烧,热水中的白磷不能燃烧;无污染;
例3、C
例4、热量;戴维灯采用一种网眼很小的普通金属网罩住火焰,由于金属能够吸收热量并散放到空气中,使金属周围的温度降低,甲烷的温度达不到着火点,所以不会引燃外界的甲烷气体
例5、(1)燃烧需要氧气 (2)红磷的着火点比白磷高,热水的温度达不到红磷的着火点
(3)①必须足量 ②密封好,多次倒置(合理即可)
3、例1、D
例2、可燃物;氧气;降低温度到可燃物的着火点以下,隔绝空气;
例3、C
例4、(1)爆炸
(2)吹散面粉,使面粉充满罐子
(3)在密闭的空间内剧烈燃烧
(4)严禁烟火;开窗通风
4、例1、D
例2、D
例3、(1)放热 (2)化合
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
