八下科学2章分析探究试题选(1)
图片预览


文档简介
八下科学第2章探究题选(1)
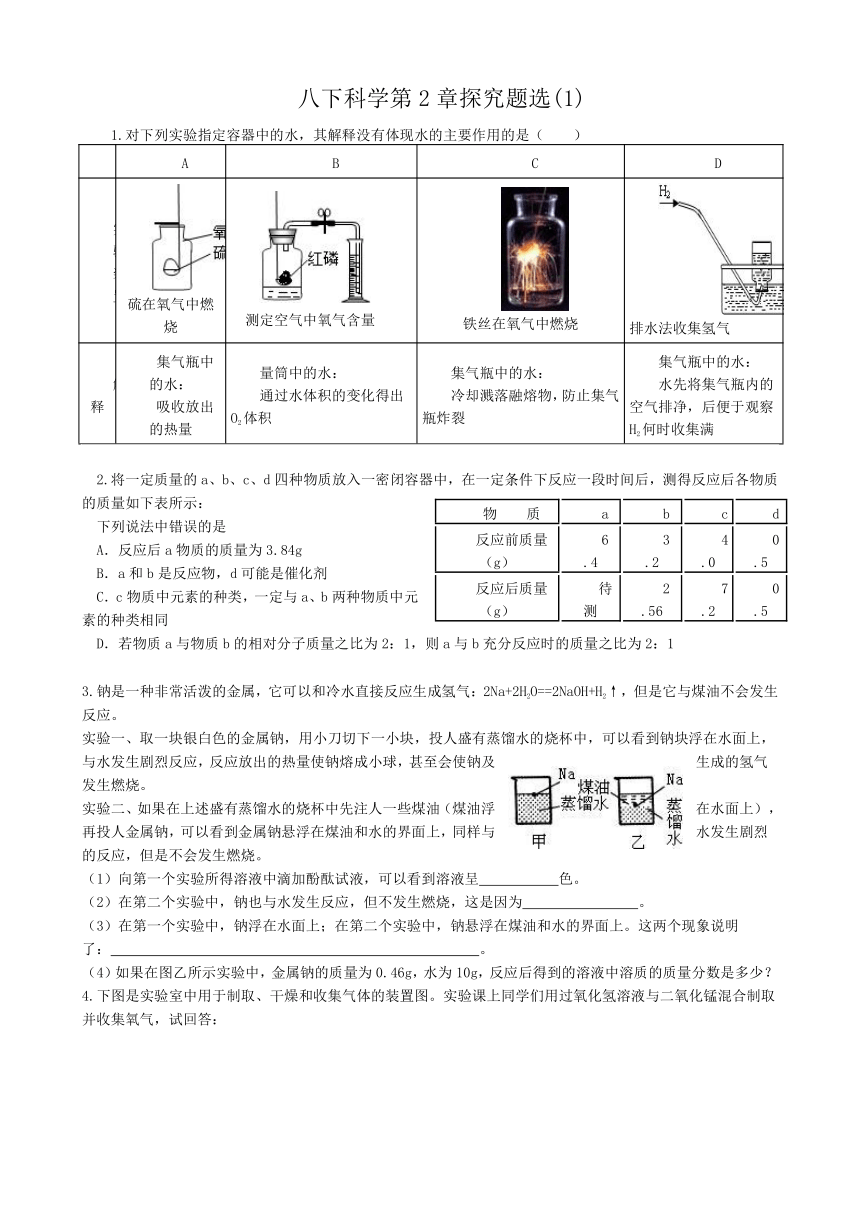
1.对下列实验指定容器中的水,其解释没有体现水的主要作用的是( )
A B C D
实验装置
硫在氧气中燃烧
测定空气中氧气含量
铁丝在氧气中燃烧
排水法收集氢气
解释 集气瓶中的水:吸收放出的热量 量筒中的水:通过水体积的变化得出O2体积 集气瓶中的水:冷却溅落融熔物,防止集气瓶炸裂 集气瓶中的水:水先将集气瓶内的空气排净,后便于观察H2何时收集满
物 质 a b c d
反应前质量(g) 6.4 3.2 4.0 0.5
反应后质量(g) 待测 2.56 7.2 0.5
2.将一定质量的a、b、c、d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量如下表所示:
下列说法中错误的是
A.反应后a物质的质量为3.84g
B.a和b是反应物,d可能是催化剂
C.c物质中元素的种类,一定与a、b两种物质中元素的种类相同
D.若物质a与物质b的相对分子质量之比为2:1,则a与b充分反应时的质量之比为2:1
3.钠是一种非常活泼的金属,它可以和冷水直接反应生成氢气:2Na+2H2O==2NaOH+H2↑,但是它与煤油不会发生反应。
实验一、取一块银白色的金属钠,用小刀切下一小块,投人盛有蒸馏水的烧杯中,可以看到钠块浮在水面上,与水发生剧烈反应,反应放出的热量使钠熔成小球,甚至会使钠及生成的氢气发生燃烧。
实验二、如果在上述盛有蒸馏水的烧杯中先注人一些煤油(煤油浮在水面上),再投人金属钠,可以看到金属钠悬浮在煤油和水的界面上,同样与水发生剧烈的反应,但是不会发生燃烧。
(1)向第一个实验所得溶液中滴加酚酞试液,可以看到溶液呈 色。
(2)在第二个实验中,钠也与水发生反应,但不发生燃烧,这是因为 。
(3)在第一个实验中,钠浮在水面上;在第二个实验中,钠悬浮在煤油和水的界面上。这两个现象说明了: 。
(4)如果在图乙所示实验中,金属钠的质量为0.46g,水为10g,反应后得到的溶液中溶质的质量分数是多少?
4.下图是实验室中用于制取、干燥和收集气体的装置图。实验课上同学们用过氧化氢溶液与二氧化锰混合制取并收集氧气,试回答:
⑴写出A图中带标号仪器的名称:①_______________,②_______________。
⑵用该方法制取氧气的化学方程式是_____________________________________。
⑶该方法制取氧气的发生装置应选择___________,若用C装置采用排水法收集氧气,进气口为____________。(填a或b)
⑷若用D装置干燥氧气,D中应盛放的试剂是___________________。
⑸甲、乙、丙三名同学用所选装置合作实验过程中,胶塞突然弹飞,并有少量的液体溅到实验台和衣服上。就此异常现象三名同学探究如下:
【问 题】为什么胶塞会突然弹飞呢?
【查阅资料】①容器内瞬间产生气体过多,压强过大,可能导致胶塞弹飞。
②化学反应速率与反应物的浓度、接触面积、温度、催化剂等因素有关。
【猜 想】甲同学:导气管堵塞或弯折造成的。乙同学:过氧化氢溶液用量过多造成的。丙同学:过氧化氢溶液的溶质质量分数过大造成的。
【分析验证】通过检查实验装置发现导气管没有堵塞、弯折的情况;与实验成功的小组同学交流,得知各小组所用过氧化氢溶液溶质的质量分数均相同。于是他们否定了____________两名同学的猜想。请你设计实验,验证另一名同学的猜想是导致本次实验胶塞弹飞的主要原因。
【交流反思】⑴老师建议他们可以通过改进发生装置的方法,避免胶塞弹飞。你对所选的发生装置有何改进设想?(语言叙述或画图均可)
⑵实验结束后,有的同学发现衣服和手上出现有白色的斑点。由此推出过氧化氢溶液还具有的一条性质________________________。
5. 右图所示的是电解水实验装置。通电一段时间后,
在两个试管中分别收集到气体a和气体b。 请回答:
①电解水时,将 能转化为化学能;②气体a为 ;
③实验室检验气体b的方法是 。
电解水的文字表达式为 ,
反应的基本类型是 。
(2)(5分)小明对妈妈杀鱼时从鱼肚内取出的鳔产生了兴趣,他决定了 “探究鳔内气体体积和成分”作为研究性学习的课题。小明通过查阅有关资料获知:这种鱼鳔内氧气约占1/4,其余主要是二氧化碳(二氧化碳能溶于水)和氮气。探究分两步进行。
①测量鳔内气体体积。小明设计了两种方法:
A.用医用注射器抽取鳔内气体,测量其体积;
B.在水下剌破鳔,用排水集气法收集鳔内气体并测量其体积(如右图)。
你认为两种方法中合理的是 ;
②探究鳔内气体的成分。给你两集气瓶的鳔内气体,请你帮助他设计实验验证假设。
验 证 方 法 现 象
鳔内含O2
鳔内含CO2
6.请结合下图所示实验装置回答有关问题:
(1)写出装置中标号仪器的名称。a ;b 。
(2)用过氧化氢溶液与二氧化锰反应制取氧气,发生装置用_______ (填序号),其反应的文字表达式是_________________________________ 。
(3)加热氯酸钾和二氧化锰的混合物制取氧气,发生装置用_______,其反应的文字表达式是_________________________________ 。
(4)如果想收集一瓶较纯净的氧气,收集气体的装置最好是__________。
(5)氨气(NH3)极易溶于水,且密度比空气小,实验室常用加热固体硫酸铵和固体熟石灰的混合物来制取氨气,应选用的发生装置是 ,收集氨气则用________装置。
(6)已知过氧化钠是一种淡黄色固体,常温下可与水反应生成氢氧化钠和氧气,如果在实验中用过氧化钠与水反应来制取氧气,应选用的气体发生装置是 ,
其反应的文字表达式是 。
7. 绿色植物的呼吸作用会产生二氧化碳,小明猜想:种子的萌发过程可能也会产生二氧化碳,他设计了如图实验装置。打开D装置中的阀门,水位下降,空气就会依次进入装置。
(1)按照实验设计意图,如果观察到C装置中澄清石灰水变浑浊现象,则小明的猜想是正确的。但思维严密的小庭却认为实验还有漏洞,她建议在 (选填:AB、BC或CD)之间再增加一个C装置,就可以弥补上图实验设计的不足,那么,改进后的实验装置中,当观察到 现象时才能证明小明的猜想是正确的。
(2)请指出D装置的一个优点: 。
A B C D
8. 某同学经查资料了解到二氧化碳会溶于水并与水发生反应生成酸。该同学设计了以下实验,验证了这一结论。
实验l:取一小块经紫色石蕊溶液浸泡过的干燥的纸(以下简称“纸修),往纸上滴上几滴稀醋酸,纸变红色。
实验2:取一小块纸.往纸上滴上几滴纯净的水,纸不变色。
实验3:
实验4:将二氧化碳通入盛有水的试管中一会儿,用胶头漓管取其中的溶液滴到纸上,纸变红
回答下列问题:
(1)实验2的目的是: ;
(2)补充实验3: ;
(3)写出二氧化碳与水反应的化学方程式: .
9.(1)学习二氧化碳性质时,老师做了如下图所示的实验。结果发现,澄清石灰水变浑浊。请写出澄清石灰水变浑浊有关反应的化学方程式_____________________。
老师提出:氢氧化钠与氢氧化钙同属于碱类化合物,与氢氧化钙的化学性质相似,那么,氢氧化钠能否与二氧化碳反应呢?
同学们围绕着这个问题,通过查阅资料得知:常温下,CO2+2NaOH=Na2CO3+H2O。
接着,在老师指导下,完成了如下实验:将上述实验中的澄清石灰水换成氢氧化钠溶液,向其中通入CO2,观察到的实验现象为_________________________。
(2)为了验证CO2能与氢氧化钠发生化学反应,同学们设计了如下实验
①甲实验:向盛满CO2的塑料矿泉水瓶(质软)中加入一定量NaOH溶液,迅速旋紧瓶塞,并振荡。静止一会儿后观察到的实验现象为___________。
②乙实验:向盛满CO2的集气瓶中倒入一定量NaOH溶液,迅速在瓶口处塞上一个去壳熟鸡蛋,静止一会儿后可观察到的实验现象为_____________。
(3)做完上述实验后,部分同学提出质疑,认为上述实验不足以说明CO2与氢氧化钠发生了化学反应。你认为这部分同学提出上述质疑,主要考虑的干扰因素是________________。为了进一步验证CO2能与氢氧化钠发生化学反应,同学们又设计了如下实验:
①A瓶盛装的试剂是________________,B瓶盛装的试剂是______________,实验时应_____[填“打开”或“关闭”]活塞K。
②进行此实验时,通入CO2的体积应_________[填“大于”、“等于”或“小于”]A瓶溶液的体积。
③能证明CO2能与氢氧化钠发生化学反应的实验现象是______________________________。
10. 学习了MnO2对过氧化氢有催化作用的知识后。某同学想:CuO能否起到类似MnO2的催化剂作用呢?于是进行了如下探究。
【猜想】Ⅰ. CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ. CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ. CuO是反应的催化剂,反应前后_________ _____________________。
【实验】用天平称量0.2gCuO,取5ml5%的过氧化氢溶液于试管中,进行如下实验:
(1)填写下表:
步骤③现象 步骤⑥结果 步骤⑦现象 结论
___ _____带火星的木条复燃 ____ _____ 溶液中有气泡放出
_____ _______ 猜想Ⅰ、Ⅱ不成立
猜想Ⅲ成立
(2)步骤①的目的________ ____________。
(3)步骤④需用到的实验仪器有:铁甲台(带铁圈)、漏斗、烧杯、_____ ____。
(4)过氧化氢能被CuO催化分解放出O2的化学方程式为___________________。
【拓展】要探究步骤⑤做过催化剂的CuO其它化学性质,还应补做的实验是______________
_____ __________________(写一种)。
11. 实验室制取氧气是初中化学阶段的重要实验。小元同学准确称取7.9g纯净的高锰酸钾加热一段时间后,收集到氧气580mL(标准状况)。(1)请写出两个实验室用固体反应物制取氧气的化学方程式: 、 。
(2)意外发现:根据化学方程式计算,7.9g高锰酸钾完全分解,应生成氧气560mL(标准状况)。小元通过数据分析,意外发现收集到的氧气体积和理论计算的氧气体积不相符合,并且在实验中还意外发现锰酸钾溶液呈墨绿色。
(3)提出假设:小元取实验后的少量固体残渣再次加热,经检验又产生了氧气。根据小元发现的问题和上述实验结果可以做出如下假设:
假设1:二氧化锰也可以受热分解产生氧气
假设2:锰酸钾也可以受热分解产生氧气
假设3:二氧化锰和锰酸钾受热都可以放出氧气
假设4:
(4)设计实验:小元用最初加热所得的残渣及必要的实验用品,设计了如下实验流程验证假设2。请在下面实验流程方框中的相应位置填写各步骤的实验操作名称。
请简要叙述步骤5的操作
。
(5)得出结论:若观察到 ,则假设2成立;若观察到 ,则假设2不成立。
12.某化学小组围绕燃烧与灭火的主题开展了相关活动。请你参与完成:
(1)从图一中观察到的现象及所得到结论正确的是 。
A.实验中烧杯里的热水只起提高温度的作用
B.水下白磷未燃烧是由于没有与氧气接触
C.实验不能比较白磷和红磷的着火点高低
D.实验说明可燃物燃烧时,温度必须达到着火点或与氧气接触
(2)改进后的装置(如图二)与图一相比,其优点是 。欲使图二中的红磷着火,可将试管从水中取出并 后才能对试管加热。
(3) 学习化学的目的并不在于要成为化学家,重要的是善于用化学知识去分析、解决生产生活中的问题。从化学的角度看,下列做法中不正确的是 。
A.家用电器着火,应先切断电源再用泡沫灭火器灭火
B.油锅着火,应迅速向锅中掺水,降低温度使其熄灭
C.大楼里着火时,应该用湿毛巾捂住口鼻,俯下身子逃出火灾区
D.室内起火时,应打开门窗,避免吸入浓烟
E.森林失火,向逆风方向奔跑逃离火灾区
13. 认识燃烧,科学地利用燃烧,使燃烧为人类服务是十分重要的。为验证可燃物燃烧的条件,某兴趣小组进行了如下探究活动。
[查阅资料]白磷的着火点是40℃,红磷的着火点是240℃,两种物质的燃烧产物五氧化二磷是白色固体,会刺激人体呼吸道,能与空气中的水蒸气反应,生成有毒的偏磷酸(HPO3)。
[设计实验]小组同学设计了下图的实验装置进行实验。
[收集证据]实验中获得了如下实验事实:
①A试管内的白磷燃烧;②热水中的白磷不燃烧;③B试管内的红磷不燃烧。
[得出结论]结论1:依据上述实验事实 (选填序号)可知:可燃物燃烧需与氧气接触。
结论2:依据上述实验事实①③可知:可燃物燃烧需满足的条件是 。
[拓展延伸]若将A试管上带玻璃管的橡皮塞换成实心橡皮塞,在实验中可能会发生的问题是: ;若去除A试管上带玻璃管的橡皮塞,在实验中又可能会出现的问题是: 。
[知识运用]我国的成语蕴含着丰富的化学知识。下面是一些与燃烧有关的成语的文学解释,请根据燃烧的条件和灭火的原理解释以下成语的化学含义。
煽风点火:比喻煽动别人闹事。 ;
釜底抽薪:抽去锅底下的柴火,比喻从根本上解决问题。 。
14. 人通过肺与外界进行气体交换,吸入空气中的氧气,排出二氧化碳和水蒸气。但人体排出的二氧化碳究竟是空气中原有的,还是人体代谢的最终产物,为了证实这个问题,有人采用了右图装置进行实验。
⑴人吸气时,应将活塞A_______(填“打开”或“关闭”),活塞B_______(同上)。
⑵人呼气时,应将活塞A_______,活塞B_______,此时可观察到Ⅱ瓶内的现象是_______。
⑶Ⅰ瓶中所装试剂的作用是_________,Ⅱ瓶中所装试剂的作用是___________。
⑷将上述操作反复进行,能证明人呼出的气体中含有的二氧化碳不是来自于______,而是来自于_____________。
15. 化学课上,同学们做了人体呼出的气体使澄清石灰水变浑浊的实验后,对呼出的气体中主要成分及含量非常好奇,设计实验进行探究。
【提出问题】呼出的气体中有哪些主要成分,它们的含量是多少?
【查阅资料】①呼出的气体中仍含有O2。
②CO2在饱和NaHCO3溶液中的溶解度非常小。
【猜想与实验】
猜想:呼出的气体中主要成分是N2、O2、CO2、水蒸气等。
实验I:验证呼出的气体中含有水蒸气。
(1)实验操作如图所示。
(2)观察到的现象为________,根据该现象可以判断呼出的气体中含有水蒸气。
实验II:验证呼出的气体中含有N2、O2、CO2,并测定其含量。
同学们在老师的指导下设计了如下图所示装置(B是带刻度的量气装置)。
(1)实验记录
实验操作 主要实验现象 实验结论及解释
① 检查装置的气密性。 向装置中加入药品。 关闭止水夹a~f。 装置的气密性良好。
② 打开b、c、d,向B中吹入一定量气体后关闭d,并冷却到室温。 B中液体进入到A中,B中液体减少500 mL。 收集500 mL气体。
③ 关闭b,打开a、e、f,用打气筒向A中缓缓充气,直到B中气体刚好全部排出。 ________,D中液体为475 mL。 反应的化学方程式为________。
④ 关闭e、f,用凸透镜聚光引燃白磷。 白磷燃烧,产生大量白烟,放出大量热。 呼出的气体中含有O2。
⑤ 待白磷熄灭并冷却到室温,打开f。 ________,D中剩余液体为400 mL。 呼出的气体中含有N2。
(2)数据处理
呼出的气体中主要成分的含量
N2 O2 CO2
体积/mL
体积分数/%
同学们经过3次重复实验,确认了呼出气体中的主要成分及其含量。
【实验反思】
(1)该实验设计依据的N2性质有 (填字母序号)。
A.难溶于水 B.不能和NaOH溶液反应
C.无色无味的气体 D.不能燃烧,也不支持燃烧
(2)实验II操作⑤中,若C中气体未完全冷却就打开f并读数,则所测O2的体积分数(填“偏小”、“不变”或“偏大”)。
16.过氧化氢溶液会自然分解,使溶质质量分数减小。为测定一瓶100 g 30%的过氧化氢溶液久置后的溶质质量分数。取该溶液27.2 g,加入适量二氧化锰,生成气体的质量与反应时间的关系如右图所示。试计算
⑴久置后,该溶液中溶质的质量分数。
⑵该瓶溶液中,已经分解的过氧化氢质量(最后结果保留一位小数)。
参考答案
1.分析:A中水主要是为了吸收反应生成的二氧化硫气体;
B中的水是为了通过水的体积变化得到氧气的体积;
C中的水是为了防止炸裂集气瓶;
D中的水是为了排出空气,便于观察氢气是否收集满.
解答:解:A中水主要是为了吸收反应生成的二氧化硫气体,不是为了吸收反应产生的热量.
故选A.
2.答:选D
3.分析:(1)2Na+2H2O=2NaOH+H2↑,属于单质+化合物→单质+化合物,故为置换反应,钠与水可以反应生成氢氧化钠,显碱性,能使酚酞变红;
(2)燃烧需同时具备三个条件,即有可燃物,可燃物与氧气接触,温度达到可燃物的着火点,,煤油在可燃物的上面,阻止了可燃物与氧气接触;
(3)煤油在最上面,钠在中间,水在下面,是由其密度决定的;
(4)要求所得溶液的溶质质量分数,须知道溶质和溶液的质量,要注意所生成的氢气不能算在所得溶液里面.
解:(1)根据钠与水反应的化学方程式,2Na+2H2O=2NaOH+H2↑,单质+化合物→单质+化合物,可以看出此反应为置换反应,生成的氢氧化钠能使酚酞变红,所以本题答案为:置换反应,红;
(2)钠与水反应产生H2,放出的热量可以达到氢气的着火点,Na或H2燃烧要同时具备两个条件,一是温度达到可燃物的着火点,二是可燃物与氧气(空气)接触.Na与水反应放出大量热(使其熔成小球),温度达到Na、H2燃烧的着火点,但是第二个实验烧杯中加入煤油,煤油密度小于水,覆盖在钠的表面,隔绝了钠与空气接触,所以在第二个实验中H2、Na不发生燃烧,所以本题答案为:可燃物未与氧气接触;
(3)钠浮在水面上,说明钠的密度比水小,煤油和水有界面,说明煤油、水不互溶,钠悬浮在煤油和水的界面上说明钠的密度比煤油大,所以本题答案为:ρ(水)>ρ(Na)>ρ(煤油),煤油、水不互溶;
(4)解:要求所得溶液的溶质质量分数,需知道溶质和溶液的质量,溶质为生成的氢氧化钠,反应生成的氢气不能算在溶液里,根据反应的化学方程式可以求出氢氧化钠和氢气的质量,进而进行求算.
设0.46gNa与水完全反应生成NaOH的质量为x,生成H2的质量为y.
2Na + 2H2O = 2NaOH + H2↑
46 80 2
0.46g x y
46:0.46g=80:x x=0.80g
46:0.46g=2:y y=0.02g
溶液中NaOH的质量分数为:
×100%≈7.7%
4.答案:
5.(1)电 (2)氢气(或H2) (3) 将带火星的木条伸入气体中,木条复燃,证明是氧气
(4)水 氢气 +氧气 分解反应
(2)A (2)用燃着的木条伸到装有该气体的集气瓶中;木条燃烧情况变化不大;向装有该气体的集气瓶中倒入澄清石灰水;澄清石灰水变浑浊。
6.(1)酒精灯;试管 (2)B ;过氧化氢溶液 水 + 氧气
(3)A ; 氯酸钾 氯化钾 +氧气 (4)C (5)A ;E
(6) B; 过氧化钠 +水 氢氧化钠 +氧气
7.答案:
(1)AB, AB之间装置中的澄清石灰水不变浑浊而BD之间装置中的澄清石灰水变浑浊
(2)可以通过控制水流的速度来控制空气通入的速度;可以收集气体;防止外界的气体从右侧进入C装置等(答出一点即可)
解析:
因为空气中也有二氧化碳,在AB之间再增加一个C装置,就可以弥补上图实验设计的不足。
8.(1)水不能使紫色石蕊变红(2)将干燥纸放入CO2中,干燥纸不变色
(3)CO2 + H2O ==H2CO3
9.答案: (1)CO2+Ca(OH)2=CaCO3↓+H2O。无明显变化。
(2)①塑料瓶变瘪 ②鸡蛋被吞入瓶中
(3)可能是CO2溶于水造成塑料瓶变瘪。
①NaOH溶液,澄清石灰水,关闭。
②大于
③A、B中均无明显现象。
10.答案:
【猜想】质量和化学性质不变
【实验】(1)有气泡产生;质量不变;产生能使带火星的木条复燃的气体(2)过氧化氢溶液自己不能分解(3)玻璃棒(4)2H2O22H2O+O2↑
【拓展】CuO+H2SO4==CuSO4+H2O
11.答案:
(1)
(不要求顺序)
(3)MnO2可以催化K2MnO4受热分解产生O2(或“K2MnO4可以催化MnO2受热分解产生O2”或“KMnO4在不同温度下以其它方式分解产生更多氧气”或“升高温度K2MnO4和MnO2相互反应产生O2”)(合理假设均给分)
(4)溶解 过滤 蒸发
取干燥后的固体于试管中充分加热,将带火星的木条(或燃烧的木条)插入试管中(2分,未表达出“充分加热”的含义扣1分,其它合理答案给分)
(5)带火星的木条复燃(木条燃烧更旺) 带火星的木条没有复燃(木条没有燃烧更旺)
12.答案:
(1)B
(2)环保 擦干
(3)ABD
解析:
物质燃烧必须满足三个条件:可燃物、与氧气(空气)接触、达到着火点.铜片上的白磷与空气接触、达到着火点,所以燃烧.铜片上的红磷没有达到着火点,所以不燃烧.水中的白磷不与氧气接触,不能燃烧.磷燃烧生成具有刺激性气味的气体,如图二装置可以防止空气的污染, 掌握各种物质的性质和灭火的方法
13.答案:
[得出结论]①②(1分) 温度需达到可燃物的着火点(1分)
[拓展延伸]试管爆裂或橡皮塞冲出(1分) 燃烧产生的五氧化二磷进入大气,造成污染(1分)
[知识运用]氧气充足时燃烧更旺(1分) 由于隔离了可燃物,所以不能继续燃烧(1分)
14.答案:
15.答案:
16. 解:⑴设27.2 g过氧化氢溶液中溶质的质量为x。
2H2O2 = 2H2O + O2↑
68 32
x 3.2 g
x=6.8 g
该溶液中溶质的质量分数=
⑵设已分解的过氧化氢的质量为y ,产生氧气的质量为z。
2H2O2 = 2H2O + O2↑
68 32
y z
z =
=25% y=5.6g
1.对下列实验指定容器中的水,其解释没有体现水的主要作用的是( )
A B C D
实验装置
硫在氧气中燃烧
测定空气中氧气含量
铁丝在氧气中燃烧
排水法收集氢气
解释 集气瓶中的水:吸收放出的热量 量筒中的水:通过水体积的变化得出O2体积 集气瓶中的水:冷却溅落融熔物,防止集气瓶炸裂 集气瓶中的水:水先将集气瓶内的空气排净,后便于观察H2何时收集满
物 质 a b c d
反应前质量(g) 6.4 3.2 4.0 0.5
反应后质量(g) 待测 2.56 7.2 0.5
2.将一定质量的a、b、c、d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量如下表所示:
下列说法中错误的是
A.反应后a物质的质量为3.84g
B.a和b是反应物,d可能是催化剂
C.c物质中元素的种类,一定与a、b两种物质中元素的种类相同
D.若物质a与物质b的相对分子质量之比为2:1,则a与b充分反应时的质量之比为2:1
3.钠是一种非常活泼的金属,它可以和冷水直接反应生成氢气:2Na+2H2O==2NaOH+H2↑,但是它与煤油不会发生反应。
实验一、取一块银白色的金属钠,用小刀切下一小块,投人盛有蒸馏水的烧杯中,可以看到钠块浮在水面上,与水发生剧烈反应,反应放出的热量使钠熔成小球,甚至会使钠及生成的氢气发生燃烧。
实验二、如果在上述盛有蒸馏水的烧杯中先注人一些煤油(煤油浮在水面上),再投人金属钠,可以看到金属钠悬浮在煤油和水的界面上,同样与水发生剧烈的反应,但是不会发生燃烧。
(1)向第一个实验所得溶液中滴加酚酞试液,可以看到溶液呈 色。
(2)在第二个实验中,钠也与水发生反应,但不发生燃烧,这是因为 。
(3)在第一个实验中,钠浮在水面上;在第二个实验中,钠悬浮在煤油和水的界面上。这两个现象说明了: 。
(4)如果在图乙所示实验中,金属钠的质量为0.46g,水为10g,反应后得到的溶液中溶质的质量分数是多少?
4.下图是实验室中用于制取、干燥和收集气体的装置图。实验课上同学们用过氧化氢溶液与二氧化锰混合制取并收集氧气,试回答:
⑴写出A图中带标号仪器的名称:①_______________,②_______________。
⑵用该方法制取氧气的化学方程式是_____________________________________。
⑶该方法制取氧气的发生装置应选择___________,若用C装置采用排水法收集氧气,进气口为____________。(填a或b)
⑷若用D装置干燥氧气,D中应盛放的试剂是___________________。
⑸甲、乙、丙三名同学用所选装置合作实验过程中,胶塞突然弹飞,并有少量的液体溅到实验台和衣服上。就此异常现象三名同学探究如下:
【问 题】为什么胶塞会突然弹飞呢?
【查阅资料】①容器内瞬间产生气体过多,压强过大,可能导致胶塞弹飞。
②化学反应速率与反应物的浓度、接触面积、温度、催化剂等因素有关。
【猜 想】甲同学:导气管堵塞或弯折造成的。乙同学:过氧化氢溶液用量过多造成的。丙同学:过氧化氢溶液的溶质质量分数过大造成的。
【分析验证】通过检查实验装置发现导气管没有堵塞、弯折的情况;与实验成功的小组同学交流,得知各小组所用过氧化氢溶液溶质的质量分数均相同。于是他们否定了____________两名同学的猜想。请你设计实验,验证另一名同学的猜想是导致本次实验胶塞弹飞的主要原因。
【交流反思】⑴老师建议他们可以通过改进发生装置的方法,避免胶塞弹飞。你对所选的发生装置有何改进设想?(语言叙述或画图均可)
⑵实验结束后,有的同学发现衣服和手上出现有白色的斑点。由此推出过氧化氢溶液还具有的一条性质________________________。
5. 右图所示的是电解水实验装置。通电一段时间后,
在两个试管中分别收集到气体a和气体b。 请回答:
①电解水时,将 能转化为化学能;②气体a为 ;
③实验室检验气体b的方法是 。
电解水的文字表达式为 ,
反应的基本类型是 。
(2)(5分)小明对妈妈杀鱼时从鱼肚内取出的鳔产生了兴趣,他决定了 “探究鳔内气体体积和成分”作为研究性学习的课题。小明通过查阅有关资料获知:这种鱼鳔内氧气约占1/4,其余主要是二氧化碳(二氧化碳能溶于水)和氮气。探究分两步进行。
①测量鳔内气体体积。小明设计了两种方法:
A.用医用注射器抽取鳔内气体,测量其体积;
B.在水下剌破鳔,用排水集气法收集鳔内气体并测量其体积(如右图)。
你认为两种方法中合理的是 ;
②探究鳔内气体的成分。给你两集气瓶的鳔内气体,请你帮助他设计实验验证假设。
验 证 方 法 现 象
鳔内含O2
鳔内含CO2
6.请结合下图所示实验装置回答有关问题:
(1)写出装置中标号仪器的名称。a ;b 。
(2)用过氧化氢溶液与二氧化锰反应制取氧气,发生装置用_______ (填序号),其反应的文字表达式是_________________________________ 。
(3)加热氯酸钾和二氧化锰的混合物制取氧气,发生装置用_______,其反应的文字表达式是_________________________________ 。
(4)如果想收集一瓶较纯净的氧气,收集气体的装置最好是__________。
(5)氨气(NH3)极易溶于水,且密度比空气小,实验室常用加热固体硫酸铵和固体熟石灰的混合物来制取氨气,应选用的发生装置是 ,收集氨气则用________装置。
(6)已知过氧化钠是一种淡黄色固体,常温下可与水反应生成氢氧化钠和氧气,如果在实验中用过氧化钠与水反应来制取氧气,应选用的气体发生装置是 ,
其反应的文字表达式是 。
7. 绿色植物的呼吸作用会产生二氧化碳,小明猜想:种子的萌发过程可能也会产生二氧化碳,他设计了如图实验装置。打开D装置中的阀门,水位下降,空气就会依次进入装置。
(1)按照实验设计意图,如果观察到C装置中澄清石灰水变浑浊现象,则小明的猜想是正确的。但思维严密的小庭却认为实验还有漏洞,她建议在 (选填:AB、BC或CD)之间再增加一个C装置,就可以弥补上图实验设计的不足,那么,改进后的实验装置中,当观察到 现象时才能证明小明的猜想是正确的。
(2)请指出D装置的一个优点: 。
A B C D
8. 某同学经查资料了解到二氧化碳会溶于水并与水发生反应生成酸。该同学设计了以下实验,验证了这一结论。
实验l:取一小块经紫色石蕊溶液浸泡过的干燥的纸(以下简称“纸修),往纸上滴上几滴稀醋酸,纸变红色。
实验2:取一小块纸.往纸上滴上几滴纯净的水,纸不变色。
实验3:
实验4:将二氧化碳通入盛有水的试管中一会儿,用胶头漓管取其中的溶液滴到纸上,纸变红
回答下列问题:
(1)实验2的目的是: ;
(2)补充实验3: ;
(3)写出二氧化碳与水反应的化学方程式: .
9.(1)学习二氧化碳性质时,老师做了如下图所示的实验。结果发现,澄清石灰水变浑浊。请写出澄清石灰水变浑浊有关反应的化学方程式_____________________。
老师提出:氢氧化钠与氢氧化钙同属于碱类化合物,与氢氧化钙的化学性质相似,那么,氢氧化钠能否与二氧化碳反应呢?
同学们围绕着这个问题,通过查阅资料得知:常温下,CO2+2NaOH=Na2CO3+H2O。
接着,在老师指导下,完成了如下实验:将上述实验中的澄清石灰水换成氢氧化钠溶液,向其中通入CO2,观察到的实验现象为_________________________。
(2)为了验证CO2能与氢氧化钠发生化学反应,同学们设计了如下实验
①甲实验:向盛满CO2的塑料矿泉水瓶(质软)中加入一定量NaOH溶液,迅速旋紧瓶塞,并振荡。静止一会儿后观察到的实验现象为___________。
②乙实验:向盛满CO2的集气瓶中倒入一定量NaOH溶液,迅速在瓶口处塞上一个去壳熟鸡蛋,静止一会儿后可观察到的实验现象为_____________。
(3)做完上述实验后,部分同学提出质疑,认为上述实验不足以说明CO2与氢氧化钠发生了化学反应。你认为这部分同学提出上述质疑,主要考虑的干扰因素是________________。为了进一步验证CO2能与氢氧化钠发生化学反应,同学们又设计了如下实验:
①A瓶盛装的试剂是________________,B瓶盛装的试剂是______________,实验时应_____[填“打开”或“关闭”]活塞K。
②进行此实验时,通入CO2的体积应_________[填“大于”、“等于”或“小于”]A瓶溶液的体积。
③能证明CO2能与氢氧化钠发生化学反应的实验现象是______________________________。
10. 学习了MnO2对过氧化氢有催化作用的知识后。某同学想:CuO能否起到类似MnO2的催化剂作用呢?于是进行了如下探究。
【猜想】Ⅰ. CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ. CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ. CuO是反应的催化剂,反应前后_________ _____________________。
【实验】用天平称量0.2gCuO,取5ml5%的过氧化氢溶液于试管中,进行如下实验:
(1)填写下表:
步骤③现象 步骤⑥结果 步骤⑦现象 结论
___ _____带火星的木条复燃 ____ _____ 溶液中有气泡放出
_____ _______ 猜想Ⅰ、Ⅱ不成立
猜想Ⅲ成立
(2)步骤①的目的________ ____________。
(3)步骤④需用到的实验仪器有:铁甲台(带铁圈)、漏斗、烧杯、_____ ____。
(4)过氧化氢能被CuO催化分解放出O2的化学方程式为___________________。
【拓展】要探究步骤⑤做过催化剂的CuO其它化学性质,还应补做的实验是______________
_____ __________________(写一种)。
11. 实验室制取氧气是初中化学阶段的重要实验。小元同学准确称取7.9g纯净的高锰酸钾加热一段时间后,收集到氧气580mL(标准状况)。(1)请写出两个实验室用固体反应物制取氧气的化学方程式: 、 。
(2)意外发现:根据化学方程式计算,7.9g高锰酸钾完全分解,应生成氧气560mL(标准状况)。小元通过数据分析,意外发现收集到的氧气体积和理论计算的氧气体积不相符合,并且在实验中还意外发现锰酸钾溶液呈墨绿色。
(3)提出假设:小元取实验后的少量固体残渣再次加热,经检验又产生了氧气。根据小元发现的问题和上述实验结果可以做出如下假设:
假设1:二氧化锰也可以受热分解产生氧气
假设2:锰酸钾也可以受热分解产生氧气
假设3:二氧化锰和锰酸钾受热都可以放出氧气
假设4:
(4)设计实验:小元用最初加热所得的残渣及必要的实验用品,设计了如下实验流程验证假设2。请在下面实验流程方框中的相应位置填写各步骤的实验操作名称。
请简要叙述步骤5的操作
。
(5)得出结论:若观察到 ,则假设2成立;若观察到 ,则假设2不成立。
12.某化学小组围绕燃烧与灭火的主题开展了相关活动。请你参与完成:
(1)从图一中观察到的现象及所得到结论正确的是 。
A.实验中烧杯里的热水只起提高温度的作用
B.水下白磷未燃烧是由于没有与氧气接触
C.实验不能比较白磷和红磷的着火点高低
D.实验说明可燃物燃烧时,温度必须达到着火点或与氧气接触
(2)改进后的装置(如图二)与图一相比,其优点是 。欲使图二中的红磷着火,可将试管从水中取出并 后才能对试管加热。
(3) 学习化学的目的并不在于要成为化学家,重要的是善于用化学知识去分析、解决生产生活中的问题。从化学的角度看,下列做法中不正确的是 。
A.家用电器着火,应先切断电源再用泡沫灭火器灭火
B.油锅着火,应迅速向锅中掺水,降低温度使其熄灭
C.大楼里着火时,应该用湿毛巾捂住口鼻,俯下身子逃出火灾区
D.室内起火时,应打开门窗,避免吸入浓烟
E.森林失火,向逆风方向奔跑逃离火灾区
13. 认识燃烧,科学地利用燃烧,使燃烧为人类服务是十分重要的。为验证可燃物燃烧的条件,某兴趣小组进行了如下探究活动。
[查阅资料]白磷的着火点是40℃,红磷的着火点是240℃,两种物质的燃烧产物五氧化二磷是白色固体,会刺激人体呼吸道,能与空气中的水蒸气反应,生成有毒的偏磷酸(HPO3)。
[设计实验]小组同学设计了下图的实验装置进行实验。
[收集证据]实验中获得了如下实验事实:
①A试管内的白磷燃烧;②热水中的白磷不燃烧;③B试管内的红磷不燃烧。
[得出结论]结论1:依据上述实验事实 (选填序号)可知:可燃物燃烧需与氧气接触。
结论2:依据上述实验事实①③可知:可燃物燃烧需满足的条件是 。
[拓展延伸]若将A试管上带玻璃管的橡皮塞换成实心橡皮塞,在实验中可能会发生的问题是: ;若去除A试管上带玻璃管的橡皮塞,在实验中又可能会出现的问题是: 。
[知识运用]我国的成语蕴含着丰富的化学知识。下面是一些与燃烧有关的成语的文学解释,请根据燃烧的条件和灭火的原理解释以下成语的化学含义。
煽风点火:比喻煽动别人闹事。 ;
釜底抽薪:抽去锅底下的柴火,比喻从根本上解决问题。 。
14. 人通过肺与外界进行气体交换,吸入空气中的氧气,排出二氧化碳和水蒸气。但人体排出的二氧化碳究竟是空气中原有的,还是人体代谢的最终产物,为了证实这个问题,有人采用了右图装置进行实验。
⑴人吸气时,应将活塞A_______(填“打开”或“关闭”),活塞B_______(同上)。
⑵人呼气时,应将活塞A_______,活塞B_______,此时可观察到Ⅱ瓶内的现象是_______。
⑶Ⅰ瓶中所装试剂的作用是_________,Ⅱ瓶中所装试剂的作用是___________。
⑷将上述操作反复进行,能证明人呼出的气体中含有的二氧化碳不是来自于______,而是来自于_____________。
15. 化学课上,同学们做了人体呼出的气体使澄清石灰水变浑浊的实验后,对呼出的气体中主要成分及含量非常好奇,设计实验进行探究。
【提出问题】呼出的气体中有哪些主要成分,它们的含量是多少?
【查阅资料】①呼出的气体中仍含有O2。
②CO2在饱和NaHCO3溶液中的溶解度非常小。
【猜想与实验】
猜想:呼出的气体中主要成分是N2、O2、CO2、水蒸气等。
实验I:验证呼出的气体中含有水蒸气。
(1)实验操作如图所示。
(2)观察到的现象为________,根据该现象可以判断呼出的气体中含有水蒸气。
实验II:验证呼出的气体中含有N2、O2、CO2,并测定其含量。
同学们在老师的指导下设计了如下图所示装置(B是带刻度的量气装置)。
(1)实验记录
实验操作 主要实验现象 实验结论及解释
① 检查装置的气密性。 向装置中加入药品。 关闭止水夹a~f。 装置的气密性良好。
② 打开b、c、d,向B中吹入一定量气体后关闭d,并冷却到室温。 B中液体进入到A中,B中液体减少500 mL。 收集500 mL气体。
③ 关闭b,打开a、e、f,用打气筒向A中缓缓充气,直到B中气体刚好全部排出。 ________,D中液体为475 mL。 反应的化学方程式为________。
④ 关闭e、f,用凸透镜聚光引燃白磷。 白磷燃烧,产生大量白烟,放出大量热。 呼出的气体中含有O2。
⑤ 待白磷熄灭并冷却到室温,打开f。 ________,D中剩余液体为400 mL。 呼出的气体中含有N2。
(2)数据处理
呼出的气体中主要成分的含量
N2 O2 CO2
体积/mL
体积分数/%
同学们经过3次重复实验,确认了呼出气体中的主要成分及其含量。
【实验反思】
(1)该实验设计依据的N2性质有 (填字母序号)。
A.难溶于水 B.不能和NaOH溶液反应
C.无色无味的气体 D.不能燃烧,也不支持燃烧
(2)实验II操作⑤中,若C中气体未完全冷却就打开f并读数,则所测O2的体积分数(填“偏小”、“不变”或“偏大”)。
16.过氧化氢溶液会自然分解,使溶质质量分数减小。为测定一瓶100 g 30%的过氧化氢溶液久置后的溶质质量分数。取该溶液27.2 g,加入适量二氧化锰,生成气体的质量与反应时间的关系如右图所示。试计算
⑴久置后,该溶液中溶质的质量分数。
⑵该瓶溶液中,已经分解的过氧化氢质量(最后结果保留一位小数)。
参考答案
1.分析:A中水主要是为了吸收反应生成的二氧化硫气体;
B中的水是为了通过水的体积变化得到氧气的体积;
C中的水是为了防止炸裂集气瓶;
D中的水是为了排出空气,便于观察氢气是否收集满.
解答:解:A中水主要是为了吸收反应生成的二氧化硫气体,不是为了吸收反应产生的热量.
故选A.
2.答:选D
3.分析:(1)2Na+2H2O=2NaOH+H2↑,属于单质+化合物→单质+化合物,故为置换反应,钠与水可以反应生成氢氧化钠,显碱性,能使酚酞变红;
(2)燃烧需同时具备三个条件,即有可燃物,可燃物与氧气接触,温度达到可燃物的着火点,,煤油在可燃物的上面,阻止了可燃物与氧气接触;
(3)煤油在最上面,钠在中间,水在下面,是由其密度决定的;
(4)要求所得溶液的溶质质量分数,须知道溶质和溶液的质量,要注意所生成的氢气不能算在所得溶液里面.
解:(1)根据钠与水反应的化学方程式,2Na+2H2O=2NaOH+H2↑,单质+化合物→单质+化合物,可以看出此反应为置换反应,生成的氢氧化钠能使酚酞变红,所以本题答案为:置换反应,红;
(2)钠与水反应产生H2,放出的热量可以达到氢气的着火点,Na或H2燃烧要同时具备两个条件,一是温度达到可燃物的着火点,二是可燃物与氧气(空气)接触.Na与水反应放出大量热(使其熔成小球),温度达到Na、H2燃烧的着火点,但是第二个实验烧杯中加入煤油,煤油密度小于水,覆盖在钠的表面,隔绝了钠与空气接触,所以在第二个实验中H2、Na不发生燃烧,所以本题答案为:可燃物未与氧气接触;
(3)钠浮在水面上,说明钠的密度比水小,煤油和水有界面,说明煤油、水不互溶,钠悬浮在煤油和水的界面上说明钠的密度比煤油大,所以本题答案为:ρ(水)>ρ(Na)>ρ(煤油),煤油、水不互溶;
(4)解:要求所得溶液的溶质质量分数,需知道溶质和溶液的质量,溶质为生成的氢氧化钠,反应生成的氢气不能算在溶液里,根据反应的化学方程式可以求出氢氧化钠和氢气的质量,进而进行求算.
设0.46gNa与水完全反应生成NaOH的质量为x,生成H2的质量为y.
2Na + 2H2O = 2NaOH + H2↑
46 80 2
0.46g x y
46:0.46g=80:x x=0.80g
46:0.46g=2:y y=0.02g
溶液中NaOH的质量分数为:
×100%≈7.7%
4.答案:
5.(1)电 (2)氢气(或H2) (3) 将带火星的木条伸入气体中,木条复燃,证明是氧气
(4)水 氢气 +氧气 分解反应
(2)A (2)用燃着的木条伸到装有该气体的集气瓶中;木条燃烧情况变化不大;向装有该气体的集气瓶中倒入澄清石灰水;澄清石灰水变浑浊。
6.(1)酒精灯;试管 (2)B ;过氧化氢溶液 水 + 氧气
(3)A ; 氯酸钾 氯化钾 +氧气 (4)C (5)A ;E
(6) B; 过氧化钠 +水 氢氧化钠 +氧气
7.答案:
(1)AB, AB之间装置中的澄清石灰水不变浑浊而BD之间装置中的澄清石灰水变浑浊
(2)可以通过控制水流的速度来控制空气通入的速度;可以收集气体;防止外界的气体从右侧进入C装置等(答出一点即可)
解析:
因为空气中也有二氧化碳,在AB之间再增加一个C装置,就可以弥补上图实验设计的不足。
8.(1)水不能使紫色石蕊变红(2)将干燥纸放入CO2中,干燥纸不变色
(3)CO2 + H2O ==H2CO3
9.答案: (1)CO2+Ca(OH)2=CaCO3↓+H2O。无明显变化。
(2)①塑料瓶变瘪 ②鸡蛋被吞入瓶中
(3)可能是CO2溶于水造成塑料瓶变瘪。
①NaOH溶液,澄清石灰水,关闭。
②大于
③A、B中均无明显现象。
10.答案:
【猜想】质量和化学性质不变
【实验】(1)有气泡产生;质量不变;产生能使带火星的木条复燃的气体(2)过氧化氢溶液自己不能分解(3)玻璃棒(4)2H2O22H2O+O2↑
【拓展】CuO+H2SO4==CuSO4+H2O
11.答案:
(1)
(不要求顺序)
(3)MnO2可以催化K2MnO4受热分解产生O2(或“K2MnO4可以催化MnO2受热分解产生O2”或“KMnO4在不同温度下以其它方式分解产生更多氧气”或“升高温度K2MnO4和MnO2相互反应产生O2”)(合理假设均给分)
(4)溶解 过滤 蒸发
取干燥后的固体于试管中充分加热,将带火星的木条(或燃烧的木条)插入试管中(2分,未表达出“充分加热”的含义扣1分,其它合理答案给分)
(5)带火星的木条复燃(木条燃烧更旺) 带火星的木条没有复燃(木条没有燃烧更旺)
12.答案:
(1)B
(2)环保 擦干
(3)ABD
解析:
物质燃烧必须满足三个条件:可燃物、与氧气(空气)接触、达到着火点.铜片上的白磷与空气接触、达到着火点,所以燃烧.铜片上的红磷没有达到着火点,所以不燃烧.水中的白磷不与氧气接触,不能燃烧.磷燃烧生成具有刺激性气味的气体,如图二装置可以防止空气的污染, 掌握各种物质的性质和灭火的方法
13.答案:
[得出结论]①②(1分) 温度需达到可燃物的着火点(1分)
[拓展延伸]试管爆裂或橡皮塞冲出(1分) 燃烧产生的五氧化二磷进入大气,造成污染(1分)
[知识运用]氧气充足时燃烧更旺(1分) 由于隔离了可燃物,所以不能继续燃烧(1分)
14.答案:
15.答案:
16. 解:⑴设27.2 g过氧化氢溶液中溶质的质量为x。
2H2O2 = 2H2O + O2↑
68 32
x 3.2 g
x=6.8 g
该溶液中溶质的质量分数=
⑵设已分解的过氧化氢的质量为y ,产生氧气的质量为z。
2H2O2 = 2H2O + O2↑
68 32
y z
z =
=25% y=5.6g
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
